מדענים מאוניברסיטת נורת'ווסטרן יצרו את הדגם המתוחכם ביותר שגדל במעבדה עד כה לחקר פגיעה בחוט השדרה האנושי.
במחקר החדש, הצוות עבד עם אורגנואידים של חוט השדרה האנושי – איברים זעירים שמקורם בתאי גזע – כדי ליצור מחדש צורות שונות של טראומה בחוט השדרה ולהעריך טיפול התחדשותי מבטיח.
בפעם הראשונה, חוקרים הראו שאורגנואידים אלה של חוט השדרה האנושיים יכולים לשחזר נאמנה את ההשלכות הביולוגיות העיקריות של פגיעה בחוט השדרה. המודל הציג מוות של תאים, דלקת וצלקות גליה, שהיא הצטברות עבה של רקמת צלקת שיוצרת מחסום פיזי וכימי המונע תיקון עצבי.
כאשר האורגנואידים הפגועים טופלו ב"מולקולות רוקדות" – טיפול ששיחזר תנועה ושיקום רקמות במחקר קודם על בעלי חיים – התוצאות היו דרמטיות. הרקמה הפגועה יצרה גדילה משמעותית של עצבים, כלומר ההרחבות הארוכות שמאפשרות לנוירונים לתקשר החלו לצמוח שוב. צלקת כמו רקמה הצטמצמה מאוד. הממצאים מוסיפים תמיכה לרעיון שטיפול זה, שקיבל לאחרונה את התואר כתרופה יתום ממינהל המזון והתרופות האמריקני (FDA), יכול לשפר את ההחלמה עבור אנשים עם פציעות בעמוד השדרה.
המחקר פורסם ב-11 בפברואר ב טבע הנדסה ביו-רפואית.
"אחד ההיבטים המרגשים ביותר של אורגנואידים הוא שאנו יכולים להשתמש בהם כדי לבדוק טיפולים חדשים ברקמות אנושיות", אמר סמואל I. Stupp של Northwestern, המחבר הבכיר של המחקר וממציא מולקולות הריקוד. "בקיצור של ניסוי קליני, זו הדרך היחידה להשיג את המטרה הזו. החלטנו לפתח שני מודלים שונים של פציעה באורגנואיד של חוט שדרה אנושי ולבדוק את הטיפול שלנו כדי לראות אם התוצאות דומות למה שראינו בעבר במודל החיה. לאחר יישום הטיפול שלנו, הצלקת הגליה דהתה באופן משמעותי והפכה בקושי ניתנת לזיהוי, וראינו את החיות הצומחות, וראינו את החיות המעצבנות. זהו אישור לכך שלטיפול שלנו יש סיכוי טוב לעבוד בבני אדם".
סטאפ היא מובילה במדעי חומרים מתחדשים ומחזיקה בתואר חבר הנאמנים פרופסור למדע והנדסת חומרים, כימיה, רפואה והנדסה ביו-רפואית ב-Northwestern. יש לו מינויים בבית הספר להנדסה מקורמיק, מכללת ויינברג לאמנויות ומדעים ובבית הספר לרפואה של פיינברג, ומנהל את המרכז לננו-רפואה מתחדשת (CRN). המחבר הראשון של המאמר הוא נוזומו טקאטה, עוזר מחקר לרפואה בפיינברג וחבר ב-CRN.
מדוע חשובים אורגנואידים אנושיים
אורגנואידים גדלים מתאי גזע פלוריפוטנטיים המושרים במעבדה. למרות שהם גרסאות מפושטות של איברים מלאים, הם דומים מאוד לרקמה אמיתית במבנה, במגוון התאי ובתפקוד. בגלל זה, אורגנואידים הם כלים רבי עוצמה לחקר מחלות, בדיקת טיפולים וחקירת האופן שבו איברים מתפתחים. הם גם מאפשרים לחוקרים לנוע מהר יותר ובעלות נמוכה יותר בהשוואה לניסויים בבעלי חיים או לניסויים קליניים בבני אדם.
בעוד שקבוצות אחרות ייצרו אורגנואידים של חוט השדרה כדי ללמוד ביולוגיה בסיסית, מודל זה מייצג התקדמות גדולה עבור חקר פציעות. האורגנואידים נמדדו מספר מילימטרים לרוחב והיו בוגרים מספיק כדי להחזיק ולדגלם נזק טראומטי.
במשך מספר חודשים, הצוות הדריך תאי גזע ליצור רקמת חוט שדרה מורכבת המכילה נוירונים ואסטרוציטים. הם גם הפכו לראשונים לשלב מיקרוגליה – תאי חיסון שנמצאים במערכת העצבים המרכזית – כדי לשכפל טוב יותר את התגובה הדלקתית הבאה בעקבות פגיעה בחוט השדרה.
"זה סוג של פסאודו-איבר," אמר סטאפ. "היינו הראשונים שהכנסנו מיקרוגליה לאורגנואיד של חוט שדרה אנושי, אז זה היה הישג עצום. זה אומר שלאורגנואיד שלנו יש את כל הכימיקלים שמערכת החיסון המקומית מייצרת בתגובה לפציעה. זה הופך אותו למודל ריאליסטי ומדויק יותר של פגיעה בחוט השדרה".
מהן מולקולות רוקדות
לאחר שהאורגנואידים של חוט השדרה פותחו במלואם, הפנו החוקרים את תשומת לבם לבדיקת פציעה וטיפול. הטיפול במולקולות רוקדות, שהוצג לראשונה בשנת 2021, משתמש בתנועה מולקולרית מבוקרת כדי לתקן רקמות ולהפוך שיתוק פוטנציאלי לאחר פגיעה טראומטית בחוט השדרה. הוא שייך לקבוצה רחבה יותר של פפטידים טיפוליים על-מולקולריים (STPs), אשר מסתמכים על מכלולים גדולים של 100,000 מולקולות או יותר כדי להפעיל קולטנים לתאים ולעורר את אותות התיקון הטבעיים של הגוף. (המושג של טיפולים על-מולקולריים משמש גם בתרופות GLP-1 הנוכחיות לירידה במשקל ולסוכרת, תחום שהמעבדה של סטאפ חקרה לפני כמעט 15 שנה.)
הטיפול מועבר כהזרקת נוזל שיוצרת במהירות רשת של ננו-סיביים הדומה למטריצה החוץ-תאית של חוט השדרה. על ידי התאמת האופן הדינמי של המולקולות נעות בתוך המבנה הזה, החוקרים שיפרו את מידת האינטראקציה האפקטיבית שלהן עם קולטני תאים המשתנים ללא הרף.
"בהתחשב בעובדה שהתאים עצמם והקולטנים שלהם נמצאים בתנועה מתמדת, אתה יכול לדמיין שמולקולות הנעות מהר יותר יתקלו בקולטנים האלה לעתים קרובות יותר", אמר סטאפ ב-2021. "אם המולקולות איטיות ולא 'חברתיות', ייתכן שהן לעולם לא יבואו במגע עם התאים".
בניסויים קודמים בבעלי חיים, זריקה בודדת שניתנה 24 שעות לאחר פציעה קשה אפשרה לעכברים ללכת שוב תוך ארבעה שבועות. ניסוחים עם תנועה מולקולרית מהירה יותר פעלו טוב יותר מגרסאות איטיות יותר, מה שמצביע על כך שתנועה מוגברת משפרת את הפעילות הביולוגית ואת האיתות הסלולרי.
הדמיית טראומה בחוט השדרה
כדי לבדוק את הטיפול, החוקרים יצרו שני סוגים נפוצים של פגיעה בחוט השדרה באורגנואידים. חלקם נחתכו באזמל כדי לחקות חתך בדומה לפצע ניתוח. אחרים ספגו פציעת חבטת דחיסה, הדומה לטראומה מפגיעת מכונית חמורה או נפילה.
שני סוגי הפציעות הובילו למוות של תאים ולהיווצרות צלקות גלייה – בדיוק כפי שקורה בפגיעה אמיתית בחוט השדרה.
"נוכל להבחין בין האסטרוציטים שהם חלק מהרקמה הרגילה לבין האסטרוציטים בצלקת הגליה, שהם גדולים ודחוסים מאוד", אמר סטאפ. "זיהינו גם ייצור של פרוטאוגליקנים כונדרויטין סולפט, שהם מולקולות במערכת העצבים המגיבות לפציעה ולמחלות".
לאחר טיפול במולקולות רוקדות, פיגום הננו-סיבי הג'ל הפחית דלקת, כיווץ צלקות גליה, גירוי את הרחבת העצבים ועודד נוירונים לגדול בדפוסים מאורגנים.
נויריטים כוללים אקסונים, אשר לעתים קרובות מנותקים בפציעות חוט השדרה. כאשר האקסונים נחתכים, התקשורת בין הנוירונים מופרעת, מה שמוביל לשיתוק ואובדן תחושה מתחת למקום הפציעה. קידום צמיחה מחודשת של עצבים יכול לחבר מחדש את המסלולים הללו ולסייע בשיקום התפקוד.
תפקידה של תנועה מולקולרית
Stupp מייחס את יעילות הטיפול לתנועה על-מולקולרית, כלומר היכולת של המולקולות לנוע במהירות ואף להתנתק לזמן קצר מרשת הננו-סיביים. ניסויים על אורגנואידים בריאים חיזקו רעיון זה.
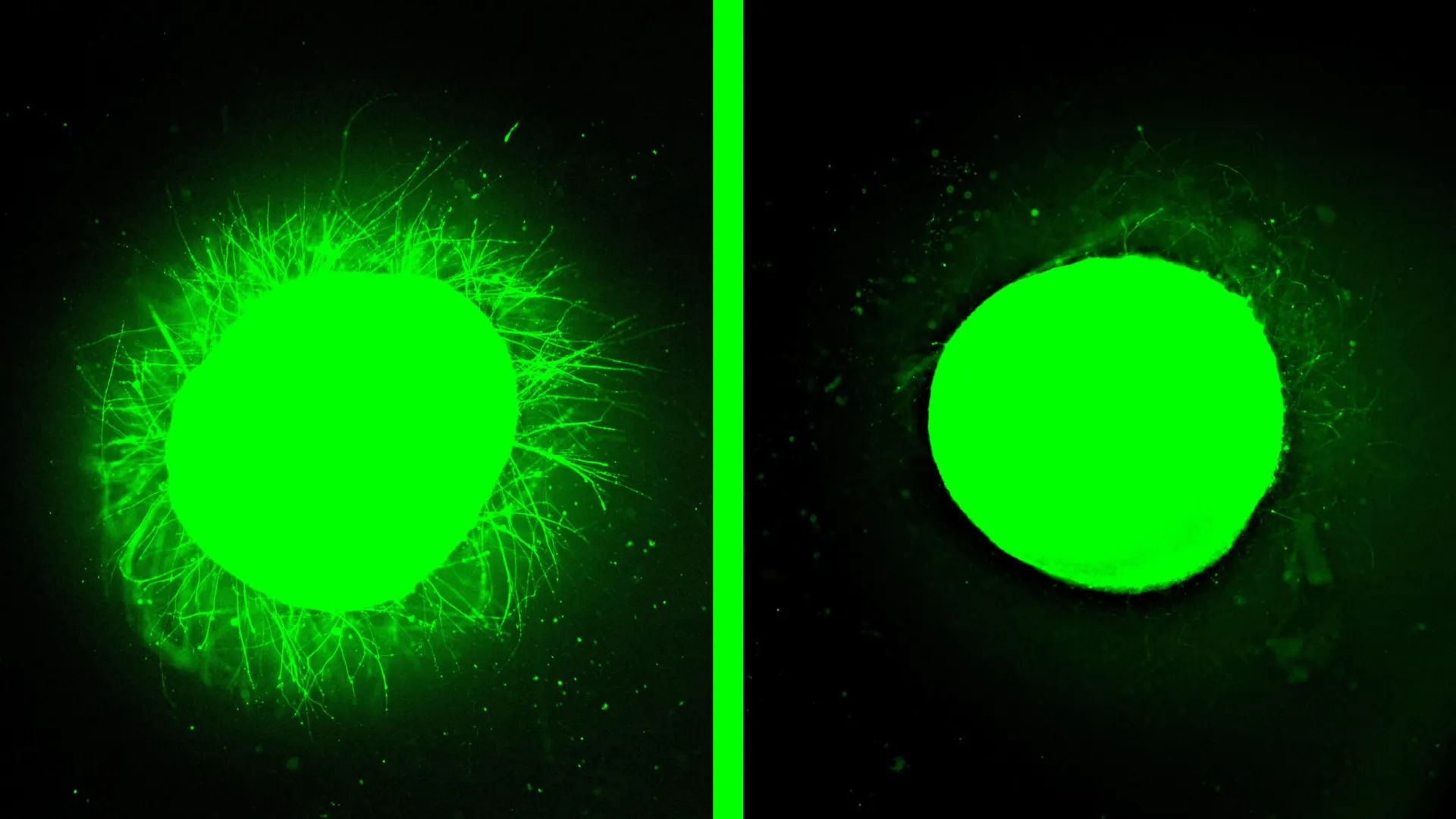
"לפני שבכלל פיתחנו את מודל הפציעה, בדקנו את הטיפול על אורגנואיד בריא", אמר. "המולקולות הרוקדות סובבו את כל הנויריטים הארוכים האלה על פני השטח של האורגנואיד, אבל כשהשתמשנו במולקולות שהן בעלות פחות או ללא תנועה, לא ראינו כלום. ההבדל הזה היה מאוד חי".
במבט קדימה, הצוות מתכנן להנדס אורגנואידים מתקדמים עוד יותר כדי לחדד את הדגמים שלהם. הם גם מתכוונים לפתח גרסאות שמשכפלות פציעות כרוניות ארוכות טווח, שכוללות בדרך כלל רקמת צלקת עבה ומתמשכת יותר. עם פיתוח נוסף, סטאפ אמר כי חוטי השדרה המיניאטוריים הללו יכולים לתרום לרפואה מותאמת אישית על ידי יצירת רקמה ניתנת להשתלה מתאי הגזע של המטופל עצמו, ולהפחית את הסיכון לדחייה חיסונית.
המחקר, "פציעה וטיפול באורגנואיד של חוט שדרה אנושי", נתמך על ידי המרכז לננו-רפואה רגנרטיבית באוניברסיטת נורת'ווסטרן ומתנת משפחת ג'ון פוטוצ'נק לחקר פציעות חוט שדרה.
קישור לכתבת המקור – 2026-02-16 14:41:00